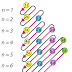
ऑफबाऊ सिद्धान्त , ऑफबाउ का नियम : इस नियम के अनुसार इलेक्ट्रॉन सबसे पहले उन उपकोशों या कोशों में होता है जिनका ऊर्जा स्तर कम होता है।
अत: यह सिद्धांत बताता है कि इलेक्ट्रॉन का वितरण कक्षा या उपकक्षा के ऊर्जा स्तर के बढ़ते हुए क्रम में होता है।
अत: स्पष्ट है कि यह नियम यह बताता है कि कोश या उपकोश में इलेक्ट्रॉन का प्रवेश किस बात पर निर्भर करता है और पहले कौनसे ऊर्जा स्तर मे इलेक्ट्रान भरा जायेगा या कक्षा या उपकक्षा में इलेक्ट्रान भरते समय किस बात का ध्यान रखना आवश्यक है।
अत: जब परमाणु में कोई इलेक्ट्रान नाभिक के चक्कर लगा रहा है तो इलेक्ट्रान पहले निम्न ऊर्जा स्तर कक्षा में जाता है या भरा जाता है उसके बाद वह इलेक्ट्रान उच्च ऊर्जा स्तर कक्षा में जाता है या भरा जाता है।
इस नियम को इस प्रकार भी परिभाषित किया जा सकता है कि जब किसी एक नए इलेक्ट्रान को किसी खाली उपकोश में भरा जाना है तो यह उस खाली उपकोश में भरा जायेगा जिसके लिए n + l का मान न्यूनतम होगा और (n+l) के बढ़ते क्रम में इलेक्ट्रान भरा जाता है।
यदि किन्ही दो उपकोश के लिए n + l का मान समान हो तो पहले इलेक्ट्रान उस उपकोश में भरा जायेगा जिसके लिए n का मान कम है।
नोट : कुछ पदार्थ या परमाणु ऐसे होते है जिनमे ऑफबाऊ सिद्धान्त की पालना नहीं होती है या कुछ अलग तरह से इलेक्ट्रान उपकोश में भरे जाते है ये परमाणु Cr , Cu , Ag , Au आदि है। इनका इलेक्ट्रॉनिक विन्यास कुछ अलग तरीके से भरा जाता है।
ऑफबाऊ सिद्धान्त के अनुसार इलेक्ट्रान के भरने का क्रम ऊर्जा स्तर का बढ़ता क्रम होता है जो निम्न प्रकार है अर्थात इलेक्ट्रान को निम्न क्रम में भरा जाता है –
1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s < 4f <5d < 6p < 7s < 5f < 6d <7p………आदि .
"....कृपया आप अपने बहुमूल्य सुझाव या प्रश्न नीचे दिए हुए टिप्पड़ी बॉक्स (Comment Box)में प्रविष्ट करें, धन्यवाद...."